エボラウイルス属
| エボラウイルス属 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
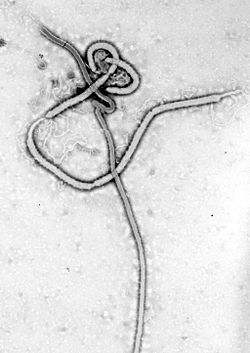 ザイールエボラウイルスの電子顕微鏡写真。
| ||||||||||||
| 分類(ウイルス) | ||||||||||||
| ||||||||||||
| 学名 | ||||||||||||
| Ebolavirus (Kuhn et. al., 2010)[1] | ||||||||||||
| タイプ種 | ||||||||||||
| ザイールエボラウイルス (Zaire ebolavirus) | ||||||||||||
| シノニム | ||||||||||||
| 和名 | ||||||||||||
| エボラウイルス | ||||||||||||
| 種 | ||||||||||||
エボラウイルス属 (英語:ebola virus) とは、モノネガウイルス目フィロウイルス科に属するウイルスの1属である。エボラ出血熱の病原体である[1]。
概要[編集 | ソースを編集]
「エボラ出血熱」も参照
エボラウイルス属は、1976年8月26日に当時のザイール(現在のコンゴ民主共和国)のエボラ川の近くの村で発見されたザイールエボラウイルス (Zaire ebolavirus) が初めての発見で[4]、44歳の男性の患者の症状で判明した。当初はマラリアを疑われたが、後に粘膜等からの出血と多臓器不全という今日で出血熱と呼ばれる症状を発症し死亡した事から、未知の感染症を疑われた[4][5]。
また、同年にはスーダンでも同じ症状の感染症が報告された。今日ではこのウイルスはスーダンエボラウイルス (Sudan ebolavirus)という別種に分類されている[6][7]。
1977年には、この2つの株が同じフィロウイルス科のマールブルクウイルス属の新種か変種ではないかと疑われていたが[8][9]、同時にまったくの新種のウイルスとしてエボラウイルスの名が提唱されていた[10]。発見後しばらくはマールブルクウイルス属と共にフィロウイルス属(Filovirus)と分類されていたが、1998年に1989年に発見されたレストンエボラウイルス(Reston evolavirus)[7]と1998年に発見されたタイフォレストエボラウイルス (Taï Forest ebolavirus) [11]と共に4種がエボラ様ウイルス (Ebola-like viruses) として分類され[2]、2002年にエボラウイルス属として定義された[3]。2010年には名称を変更せず再定義されている[1]。
種類[編集 | ソースを編集]
犬にもチベタン・マスティフからチワワまで様々な種類が存在するように、エボラウイルスにも様々な種類がある。現在は以下の5種類に分類されている。
なかでも、ザイール、スーダン、ブンディブギョの3種は、アフリカにおいてエボラ出血熱の大きなアウトブレイクを起こしてきた。
一方で、アイボリーコーストとレストンについては、これまでヒトでの大きなアウトブレイクは起きていない。ただし、家畜などに感染し壊滅的な被害を出している。
名称[編集 | ソースを編集]
エボラウイルス属は発見からしばらくは確立した分類がされてなかった。2000年に最初に発見されたウイルスはザイールエボラウイルス(zaire ebola viru, ZEV)と命名された[2]。2005年には英名は "Zaire ebolavirus" と改められた[3]。
しかし多くの論文ではザイールエボラウイルスを指してエボラウイルス (ebola virus) を用いるか、もしくは平行して使っていた。このため2010年にはエボラウイルスの名称が復活している[1]。
ウイルスの分類に関する国際委員会 (International Committee on Taxonomy of Viruses) では、エボラウイルス属を指す場合には先頭を大文字にし斜体にした「"Ebolavirus"」を用い、種小名は「"ebolavirus"」と小文字で書かなければならないとしている。エボラウイルス属自体の名称は2002年に初めて使われている。
以上の事からエボラウイルス属に関わる文章では何を指して用いているかに注意する必要がある[1]。特に日本語の文章では大文字小文字による区別は利用できないので文脈から正しく読み取る必要がある。
特徴[編集 | ソースを編集]
エボラウイルス属は重複の多いマイナス1本鎖RNAウイルスで[1]、フィロウイルス科に共通する特徴である糸状に集合した粒であるビリオンを持つ。糸は大抵曲がっており、U型、6型、杖型、コイル型などと様々な形で呼ばれている。また、分岐している場合もある。幅は80nm程度であるが、長さは974nmから1086nmである。マールブルクウイルス属の長さは795nmから828nmであり、これと比べるとやや長い。また、培養環境では最大で14000nmの長さに達する[12][13]。
ヒトとヒト以外の霊長類に対して非常に感染力が強く、ヒトの致死率はザイールエボラウイルスで約90%、スーダンエボラウイルスで約50%に達する極めて致死性の強い病原体である[14]。また、サル、ゴリラ、チンパンジーに対してもしばしば致命的となる人獣共通感染症である。
ただし、レストンエボラウイルスだけは、霊長類への感染が報告されており、ヒトからも抗体が発見されているが、その症状はなく、感染してもヒトに対して病原体となるかは今のところ不明である[4]。
2011年になって2つの独立した研究グループが、ヒトの遺伝子のうちNPC1 (Niemann-Pick disease, type C1) と呼ばれる遺伝子がコードしているタンパク質が、エボラウイルス属の感染に必須な事が示された[15][16]。
エボラウイルス属の遺伝子変化の速度はインフルエンザウイルスの100倍以上遅い。これはB型肝炎ウイルスと同程度である。マールブルクウイルス属との分化は数千年前程度と考えられている[17]。初めはマールブルクウイルス属と誤解されたものの、実際には遺伝子レベルで50%ほどマールブルクウイルス属と異なる。また抗原交差反応性もほとんど示さない[1]。
自然界での正確な分布は不明だが、アフリカ大陸で最初の感染が報告された事、5種のうち4種が人獣共通感染症であることから、アフリカの野生生物がホストであると考えられている。フィリピンでのカニクイザルに感染していたレストンエボラウイルスは自然界でのホストと考えられており、アメリカ合衆国とイタリアに輸出されているが、それらの国や周辺において自然界においては発見されていない[4]。
感染[編集 | ソースを編集]
エボラウイルス属は、血液や精液、母乳、汗を含むすべての体液から感染することが知られている。同じように血液などの体液から感染するHIVやB型肝炎ウイルスと違い、エボラウイルスは汗にも含まれている。 [18]
患者の体液が小さなキズがついた皮膚や粘膜から侵入して感染する。
エボラウイルスに感染した動物に触れたり、生食した場合には感染する可能性がある。 [19]
スーダンエボラウイルス[編集 | ソースを編集]
スーダンエボラウイルスについては2000~2001年にウガンダでの発生で飛沫感染した疑いがある。 [20]
レストンエボラウイルス[編集 | ソースを編集]
レストンエボラウイルスについては飛沫感染あるいは空気感染の疑いもある。
ザイールエボラウイルス[編集 | ソースを編集]
ザイールエボラウイルスについては、実験感染サルから3メートル離した未感染の対照サルにも伝播し、これがエアロゾルによる感染の可能性が高いという成績が報告されている。
この実験では筋肉内にエボラウイルス、ザイール株(メインガ株)をアカゲザルに接種した結果、7ー13日で死亡し、これらの実験感染サルのケージから約3メートル離したケージ内に入れられていた対照サル3頭が実験感染サルが最後に死亡した日から10日ー11日目に死亡したという結果になった。
そしてウイルスがこれらのサルの肺を含めたいろいろな組織から分離されていた。
すべての実験操作や飼育管理は対照サルから行っており、人為的な面で対照サルへの感染の起きた可能性は考えられず、エアロゾル感染がもっとも可能性が高いという結論に至っている。 [21]
またカナダ保健省でも類似の実験結果が報告されている。 [22]
その他[編集 | ソースを編集]
その他の種については今のところ空気感染を示唆する所見は確認されていない。 [23]
扱い[編集 | ソースを編集]
エボラウイルス属のウイルスは、症状が確認されていないレストンエボラウイルスを除いてヒトに対する感染力が強く、致死率も高く、有効な治療法もワクチンも存在しない。この事からエボラウイルス属はバイオセーフティレベルで最高レベルの4に指定され、扱われる施設は限られている[24]。
日本においては、エボラ出血熱は感染症の予防及び感染症の患者に対する医療に関する法律の1類感染症に指定されており、病原体としてはエボラウイルス属の種全てが指定されている。感染例の全件が直ちに届出を必要とする。これは病原体であるエボラウイルス属の検出がない場合でも、症状や所見から感染が疑われる場合も含まれる[14]。
症状[編集 | ソースを編集]
エボラ出血熱は、急性のウイルス性疾患で、しばしば、発熱、激しい衰弱、筋肉痛、頭痛、咽頭痛が突然現れる。 この初期症状は他の感染症でも頻繁に見られ、最初の数日で患者がエボラウイルス属に感染しているのを見極めるのは困難である。
これらの症状に続いて、嘔吐、下痢、発疹、腎障害、肝機能障害がみられ、内出血と外出血がみられることもある。ただし、出血熱の名の由来である外部への出血は一部の患者にしか見られない[4]。検査所見では、白血球の減少、血小板の減少、肝臓の酵素の上昇がみられる。
エボラウイルスに感染した人の血液や分泌物にウイルスが存在する間は、他の人に感染する可能性がある。実験室でエボラウイルスに感染した事例では、発症から61日目まで精液からエボラウイルスが分離された事例がある。
潜伏期間(感染から発症するまでの期間)は2日から21日とされ、エボラ出血熱のアウトブレイクの致死率は25%から90%と高い。なお、死亡せずに治癒しても失明などの重篤な障害が残ることが多い。 [25]
診断[編集 | ソースを編集]
マラリア、腸チフス、細菌性赤痢、コレラ、レプトスピラ症、ペスト、リケッチア症、回帰熱、髄膜炎、肝炎、他のウイルス性出血熱との鑑別診断を必要とする。
エボラウイルス感染の確定診断をつけられるのは、研究所で実施される数種類の異なる検査のみである。その検査方法は以下である。
- 酵素免疫測定(ELISA)法
- 抗原検出法
- 血清中和試験
- 逆転写ポリメラーゼ連鎖反応(RT-PCR)法
- 細胞培養によるウイルス分離
患者から採取した検体は、バイオハザードを引き起こす危険性が非常に高く、バイオセーフティレベルが最も高い環境下([P4施設]])でのみ取り扱うべきであるとされるが、残念ながら日本にはP4施設がない。
治療[編集 | ソースを編集]
重症例に対しては、集中的な支持療法が必要となる。患者は、しばしば脱水症状を起こし、電解質を含んだ輸液や経口補水液の投与が必要となる。
2014年8月現在、エボラ出血熱に対する特定的な治療やワクチンはない。数種類の新しい薬物療法は、実験室での研究では有望な結果が出ており、現在は評価が行われている。これらの治療薬やワクチンは実用化までに何年もかかる見込みである。
エボラウイルスの自然宿主[編集 | ソースを編集]
アフリカでは、オオコウモリ科の、特にウマヅラコウモリ(Hypsignathus monstrosus)、フランケオナシケンショウコウモリ(Epomops franqueti)、コクビワフルーツコウモリ(Myonycteris torquata)がエボラウイルスの自然宿主と考えられている。結果として、エボラウイルスの地理的分布は、オオコウモリの生息域に重なると考えられている。
動物のエボラウイルス[編集 | ソースを編集]
人以外の霊長類が人への感染源になっているが、その霊長類がウイルスの保有宿主なのではなく、むしろ人間と同様に偶発的に宿主になったと考えられている。
1994年以降、ザイールエボラウイルスとアイボリーコーストエボラウイルスによるアウトブレイクでは、チンパンジーとゴリラへの感染がみられた。
レストンエボラウイルスは、1989年、1990年、1996年に、フィリピンで飼育され、米国に輸入されたマカクサル(カニクイザル)で重症のウイルス性出血熱のアウトブレイクが起きた。また、1992年には、フィリピンからイタリアに輸入されたサルでも発生した。
2008年以降、レストンエボラウイルスは、ブタで致死的な疾患の集団発生を起こしている。ブタでは無症候性感染が報告されており、ブタは実験的なウイルス接種では発症しない傾向にある。
予防[編集 | ソースを編集]
家畜でのレストンエボラウイルスのコントロール[編集 | ソースを編集]
2014年8月現在、動物に使用できるエボラレストンウイルスに対するワクチンはない。
ブタやサルの飼育場の日常的な清掃と消毒(次亜塩素酸ナトリウムや他の洗剤による)がウイルスの失活化に有効と考えられている。これはインフルエンザウイルスやノロウイルスなどと同じである。
アウトブレイクが疑われた場合には、すぐに建物を隔離する必要がある。動物から人への感染する危険性を減らすために、死体の埋火葬を厳密に管理し、動物の殺処分が必要であれば行う。感染した動物が発見された農場の動物を他の地域に移動することを制限したり、禁止したりすることで、疾患の拡大を抑えることができると考えられている。
ブタとサルのレストンエボラウイルスのアウトブレイクは、人の感染に先行してきたので、獣医と人の公衆衛生当局に早期警報を提供するためには、新しい事例を発見するための積極的な動物健康監視システムの設立が欠かせない。
人でのエボラウイルス感染のリスクの減少[編集 | ソースを編集]
2014年8月現在、ヒトに使用できるエボラレストンウイルスに対するワクチンはない。よってヒトでの感染と死亡を減らすためには、エボラウイルスに感染する危険因子の認識の向上と、個人ができる予防対策を行うことしかできない。
アフリカでは、エボラ出血熱のアウトブレイクが発生している間、リスクを減らすために、公衆衛生学的な啓発メッセージはいくつかの要因に焦点があてられるべきである。
- エボラウイルスに感染したオオコウモリやサルとの接触や、生肉を食べることによる、野生動物から人への感染リスクの減少。動物は、手袋や、その他の適切な防護服を着用して取り扱うべきです。その産物(血と肉)は、食べる前に完全に加熱調理すべきである。
- エボラウイルスに感染した患者、特に患者の体液に直接接触または濃厚接触した人に感染者が発生している地域における、人から人への感染リスクの減少。エボラ出血熱の患者との身体的な濃厚接触は避けるべき。自宅で病気の患者の世話をする時には、手袋や適切な個人防護具を着用する。自宅で病気の患者の世話をした後と同様、病院に病気の親類を見舞った後にも、常に手洗いが必要である。
- エボラ出血熱が発生している地域では、住民に、病気の性質や、死体の埋葬を含むアウトブレイクを封じ込めるための対策を伝える必要がある。エボラ出血熱の死亡者は、迅速かつ安全に埋葬すべきである。
- アフリカでは、オオコウモリとの接触で養豚場が感染し、ウイルスを増幅してエボラ出血熱のアウトブレイクを起こすことを避けるために予防対策が必要である。
レストンエボラウイルスについての公衆衛生学的な啓発メッセージは、危険な畜産やと殺方法、危険な鮮血、生乳、動物の組織の飲食の結果として起こる、ブタから人への感染リスクを減らすことに焦点があてられるべきである。病気にかかった動物や、その組織を扱う時や、動物を屠殺する時には、手袋や、その他の適切な防護服を着用するべきである。これまでに、ブタで、レストンエボラウイルスの感染事例が報告・検出された地域では、すべての動物の製品(血、肉、乳)は、飲食する前に、完全に加熱調理すべきである。
医療機関での感染予防[編集 | ソースを編集]
エボラウイルスの人から人への感染は、主に血液や体液への直接接触と関連する。適切な感染予防対策が取られていなかった医療従事者の感染が報告されている。
エボラウイルスに感染したと確定された患者や、その疑いのある患者の診療をする医療従事者は、患者の血液や体液からの感染や、汚染された可能性のある環境に直接接触することによる感染を防ぐために感染予防策を実施するべきである。したがって、エボラウイルスに感染したと確定された患者や疑いのある患者の診療をする医療従事者は、特別な予防方法と標準予防策の強化、特に基本的な手指衛生や個人防護具の使用、安全な注射手技、安全な埋葬方法を実施することが必要となる。
検査施設の勤務者もリスクはある。エボラウイルス感染が疑われる人や動物から、診断のために採取された検体は、トレーニングを受けた職員が取り扱うべきであり、十分に設備が整った検査施設で処理すべきでる。
WHOの対応[編集 | ソースを編集]
WHOは、疾患の調査や感染拡大防止を支援するために、専門的な知識や文書を提供することによって、過去のすべてのエボラ出血熱のアウトブレイクに関わってきた。
エボラ出血熱と確定された患者や疑いのある患者を診療する際に推奨する感染予防法は、2008年3月の「フィロウイルスによる出血熱(エボラ、マールブルグ)と確定された患者や、その疑いのある患者を診療する際に、暫定的に推奨する感染予防法(Interim infection control recommendations for care of patients with suspected or confirmed Filovirus (Ebola, Marburg) haemorrhagic fever)」の中で示している。
WHOは、医療における標準予防策に関する覚書を作成した。標準予防策は、血液に由来する感染や、他の病原体による感染のリスクを減らすためのものである。標準予防策が、常に実施されていれば、血液や体液からの感染のほとんどが予防できると考えられている。標準予防策は、感染状況にかかわらず、すべての患者の医療に推奨される。標準予防策には、基本的な感染予防方法が含まれ、手指衛生、血液や体液との直接接触を避けるために個人防護具の使用、針刺しや鋭利な医療器具による傷の予防、環境管理が含まれる。
主なエボラ出血熱の発生(2012年5月現在)[編集 | ソースを編集]
| 年 | 国 | ウイルス | 患者数 | 死亡者数 | 致死率 |
| 2011 | ウガンダ | スーダンエボラウイルス | 1 | 1 | 100% |
| 2008 | コンゴ民主共和国 | ザイールエボラウイルス | 32 | 14 | 44% |
| 2007 | ウガンダ | ブンディブギョエボラウイルス | 149 | 37 | 25% |
| 2007 | コンゴ民主共和国 | ザイールエボラウイルス | 264 | 187 | 71% |
| 2005 | コンゴ共和国 | ザイールエボラウイルス | 12 | 10 | 83% |
| 2004 | スーダン | スーダンエボラウイルス | 17 | 7 | 41% |
| 2003 (11月-12月) | コンゴ共和国 | ザイールエボラウイルス | 35 | 29 | 83% |
| 2003 (1月-4月) | コンゴ共和国 | ザイールエボラウイルス | 143 | 128 | 90% |
| 2001-2002 | コンゴ共和国 | ザイールエボラウイルス | 59 | 44 | 75% |
| 2001-2002 | ガボン | ザイールエボラウイルス | 65 | 53 | 82% |
| 2000 | ウガンダ | スーダンエボラウイルス | 425 | 224 | 53% |
| 1996 | 南アフリカ(ガボンからの輸入例) | ザイールエボラウイルス | 1 | 1 | 100% |
| 1996 (7月-12月) | ガボン | ザイールエボラウイルス | 60 | 45 | 75% |
| 1996 (1月-4月) | ガボン | ザイールエボラウイルス | 31 | 21 | 68% |
| 1995 | コンゴ民主共和国 | ザイールエボラウイルス | 315 | 254 | 81% |
| 1994 | コートジボワール | アイボリーコーストエボラウイルス | 1 | 0 | 0% |
| 1994 | ガボン | ザイールエボラウイルス | 52 | 31 | 60% |
| 1979 | スーダン | スーダンエボラウイルス | 34 | 22 | 65% |
| 1977 | コンゴ民主共和国 | ザイールエボラウイルス | 1 | 1 | 100% |
| 1976 | スーダン | スーダンエボラウイルス | 284 | 151 | 53% |
| 1976 | コンゴ民主共和国 | ザイールエボラウイルス | 318 | 280 | 88% |
関連項目[編集 | ソースを編集]
参考文献[編集 | ソースを編集]
- ↑ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 Proposal for a revised taxonomy of the family Filoviridae: classification, names of taxa and viruses, and virus abbreviations Archives of Virology
- ↑ 2.0 2.1 2.2 taxonomy--San Diego 1998 Archives of Virology
- ↑ 3.0 3.1 3.2 ICTV at the Paris ICV: Results of the Plenary Session and the Binomial Ballot Archives of Virology
- ↑ 4.0 4.1 4.2 4.3 4.4 Questions and Answers about Ebola Hemorrhagic Fever Center for Disease Control and Prevention
- ↑ Clinical Aspects of Ebola Virus Disease at the Ngaliema Hospital, Kinshasa, Zaire, 1976
- ↑ Ebola haemorrhagic fever. The Lancet 377
- ↑ 7.0 7.1 Known Cases and Outbreaks of Ebola Hemorrhagic Fever, in Chronological Order Center for Disease Control and Prevention
- ↑ Isolation of Marburg-like virus from a case of haemorrhagic fever in Zaire. Archives of Virolog
- ↑ Viral haemorrhagic fever in southern Sudan and northern Zaire. Preliminary studies on the aetiological agent. Archives of Virolog
- ↑ Isolation and partial characterisation of a new virus causing acute haemorrhagic fever in Zaire. Archives of Virolog
- ↑ Ebola Cote D'Ivoire Outbreaks Stanford University
- ↑ Filoviridae: a taxonomic home for Marburg and Ebola viruses? Archives of Virolog
- ↑ Differentiation of filoviruses by electron microscopy. Archives of Virolog
- ↑ 14.0 14.1 エボラ出血熱 厚生労働省
- ↑ Ebola virus entry requires the cholesterol transporter Niemann-Pick C1 Archives of Virolog
- ↑ Small molecule inhibitors reveal Niemann-Pick C1 is essential for ebolavirus infection Archives of Virolog
- ↑ The origin and evolution of Ebola and Marburg viruses. Archives of Virology
- ↑ WEST AFRICAEbola Outbreak - CDC
- ↑ エボラ出血熱が過去最大のアウトブレイク! 日本で感染の可能性は?
- ↑ IDWR 2002年第32週号(2002年8月5日~8月4日)
- ↑ 山内一也東京大学名誉教授 人獣共通感染症連続講座 第30回 1996年2月21日
- ↑ カナダ保健省 空気感染は否定出来ない
- ↑ レストンエボラウイルス (IASR Vol. 32 p. 191-192: 2011年7月号)
- ↑ Ebola Virus Baylor College of Medicine
- ↑ FORTH|最新ニュース|2012年|エボラ出血熱について(ファクトシート)|厚生労働省検疫所
- ↑ WHO Ebola haemorrhagic fever Fact sheet August 2012